¿Existirá alguna relación entre lo que ves en las imágenes?
https://comefruta.es/wp-content/uploads/limones_4.jpg
https://static01.nyt.com/images/2017/02/15/science/15tb-flowers01/15tb-flowers01-master1050.jpg
https://pbs.twimg.com/media/Bx3ThztCMAQ1toL.jpg
https://hdstatic.net/gridfs/holadoctor/625x470__0_30-1464374356,953.jpg
https://perfumeriaspigmento.com.ar/media/catalog/product/cache/image/620x678/e9c3970ab036de70892d86c6d221abfe/8/7/87947.jpg
https://cdns3-2.primor.eu/63000-thickbox/quitaesmalte-sin-acetona.jpg
https://cdn.palbin.com/users/25610/images/blog/gallery/Limpiar-pantallas-con-alcohol-isopropilico.jpg
Quizás si lo pensamos desde la QUÍMICA de sus componentes
¿Qué coincidencias encuentras?
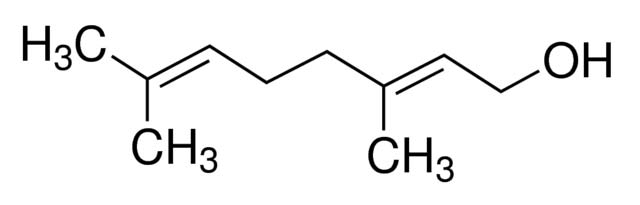
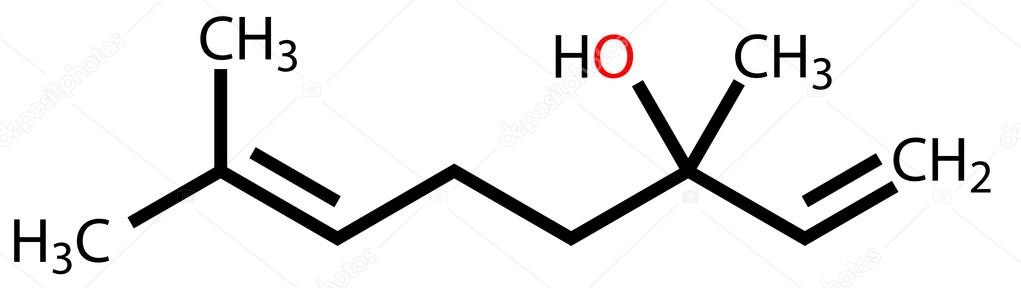
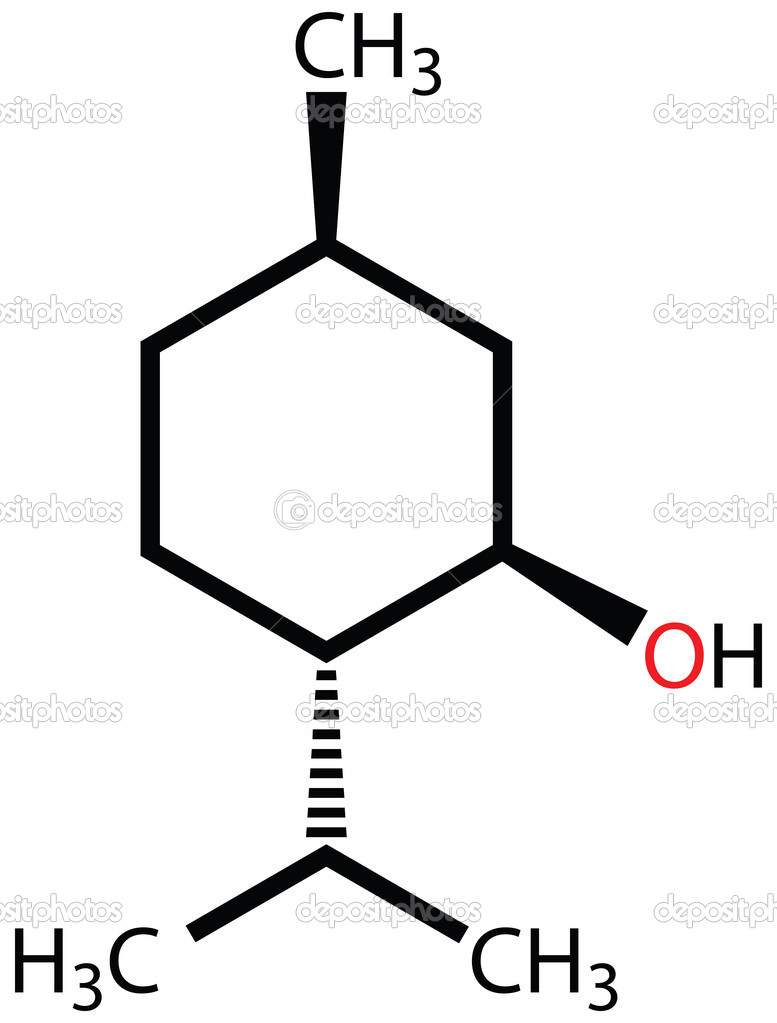
Para ello, observa las siguientes fórmulas:
https://2.wlimg.com/product_images/bc-full/dir_2/48505/geraniol-1686644.jpg
https://st.depositphotos.com/1723045/1343/v/950/depositphotos_13437744-stock-illustration-linalool-a-compound-with-pleasant.jpg
https://images-na.ssl-images-amazon.com/images/I/51BUzWDSN4L._SX342_.jpg
https://st.depositphotos.com/1723045/1325/v/950/depositphotos_13259586-stock-illustration-menthol-structural-formula.jpg
https://previews.123rf.com/images/molekuul/molekuul1404/molekuul140400013/27509737-el-alcohol-etanol-alcohol-et%C3%ADlico-mol%C3%A9cula-estructura-qu%C3%ADmica-renderizados-en-2d-estilizadas-y-f%C3%B3rmulas-esque.jpg
https://acidoclorhidrico.org/wp-content/uploads/2018/06/metanol-formula.jpg
https://esacademic.com/pictures/eswiki/50/2-propanol.png
REVISANDO UN POCO DE HISTORIA
https://lasbrujastequeremosayudar.files.wordpress.com/2016/07/billedcawrf26tix6.gif?w=620
El descubrimiento exacto de lo que hoy se conoce como “alcohol” es relativamente
incierto, hay quienes lo atribuyen a un acontecimiento accidental, probablemente
originado en la edad de piedra tardía (hace aproximadamente unos 10.000 años) cuando
alguno de nuestros antepasados probó el contenido de un tarro con miel que había sido
olvidado durante un periodo de tiempo prolongado, con lo cual, el catador quedó
expuesto a los efectos de una bebida que por la exposición natural al ambiente fue
fermentada. Las sensaciones percibidas por éste individuo, conllevarían a que
nuevamente se repitiera la experiencia (Vallee, 1998).
Con el establecimiento de la agricultura se dió paso a la fermentación de granos, proceso
que pudo originarse cerca de las fértiles deltas de Egipto y Mesopotamia. Numerosas
experimentaciones naturales debieron permitir el perfeccionamiento de la fabricación de
bebidas alcohólicas, al punto que en 6.000 A.C. los Armenios ya cultivaban la vid para la
elaboración de vino (Vallee, 1998).
Pese al aparente adelanto en la fabricación de éste tipo particular de bebidas, aún no se
tenían mecanismos idóneos para cubrir con la demanda de agua para consumo humano,
con lo cual, los problemas de enfermedades asociadas a la ingestión de la misma fueron
muy recurrentes: la disentería, el cólera y el tifus, por ejemplo; e incluso, la contaminación
de las fuentes hídricas por acción de los desechos humanos; impulsaron el consumo de
alcohol, convirtiéndolo en el único medio seguro de hidratación. Era más sano beber vino
que agua; un ejemplo claro lo vislumbramos en los viajes de Cristóbal Colón, para los
cuales se almacenó cerveza en lugar de agua dentro de las provisiones (Vallee, 1998).
Hechos como el precedente, llevaron a los medievales a denominar el alcohol como el
aqua vitae “agua de vida”.
Debido a las propiedades físicas que se le atribuyeron al alcohol como antiséptico e
hidratante, éste comenzó a ganar más y más adeptos, razón por la que las personas de
todas las edades comenzaron a consumir el alcohol con una mayor frecuencia. Con el
mejoramiento de la destilación del alcohol, se logró posesionar las bebidas alcohólicas
como la mejor opción para satisfacer el requerimiento diario de líquidos. Una forma de
fabricar la cerveza se esboza en algunas tablas de arcilla babilónicas con más de 6.000
años de antigüedad. En ellas se aprecia como se fabricaba el akratidzomai, “el
desayuno”, un tipo de cerveza sin diluir que consumían constantemente; o el siraku
sumerio, un poco más reciente, sobre los 4.000 años, época por la cual se sitúa una
tablilla farmacopea en la cual se muestran los beneficios medicinales que ostentaba el
alcohol. Estas expresiones son muestra de la importancia de ésta bebida para las
civilizaciones antiguas.
Como consecuencia de los deficientes procesos de destilación alcohólica antiguos, las
bebidas con que se contaba en ese entonces, turbarían el olfato de un enólogo moderno,
pues, además del precioso etanol, se encontraba gran cantidad de ácido acético y otros
ácidos orgánicos, con lo cual, la degustación del vino tradicional correspondería con un
trago de vinagre o sidra actual.
No fue sino hasta los años 700 de la era cristiana cuando se comenzó a desarrollar un
proceso de destilación más eficaz. El inicio se atribuye a los alquimistas árabes, quienes
denominaron al producto de la destilación como al kuhl que traducía –polvo finamente
dividido-. Debido a la adopción de muchos términos árabes por parte de los europeos,
con los correspondientes problemas de pronunciación, la denominación de al-kuhl fue
erróneamente traducida a . Como consecuencia de la naturaleza volátil del
alcohol también recibió el apelativo de ; a los alquimistas árabes les llamaba la
atención la forma como algunas sustancias liberaban “espíritus”, incluso a temperatura
ambiente, entre ellas el vino, razón por la cual también se le conoció como nombre introducido por Paracelso debido a los vapores producidos por éste.
Según Asimov (s.f.) se tiene: “cuando un líquido se evapora, parece pulverizarse hasta
desvanecerse, así que los espíritus también fueron llamados «alcohol» y los alquimistas
hablaban del «alcohol del vino» y ya en el siglo XVII la palabra «alcohol» se utilizaba
únicamente para referirse a los vapores emitidos por el vino”.
Con el perfeccionamiento de las técnicas de destilación, se logró sobrepasar el nivel
máximo de fermentación del 16% a valores un tanto superiores. El método árabe de
destilación se difundió por Europa, comenzando en Salerno donde ya se elaboraban dos
tipos distintos de bebidas: el aqua ardens (aguardiente) con una graduación alcohólica de
60° y el aqua vitae (agua de vida) con 90° (Blanco, et al., s.f.) sobre los 1100 D.C.. Desde
allí se distribuyeron de Asia Menor hacia Occidente los métodos químicos y médicos de
utilización del alcohol destilado. Posteriormente Hieronymus Brunshwig médico alsaciano
describió el proceso en el Liber de arte distillandit, primera obra impresa sobre la
destilación en el año de 1.500 (Vallee, 1998), aunque existe evidencia de que Ramón
Liull (1233-1315) puede haber sido la primera persona en elaborar un texto expositor de
ésta técnica (De aqua-vitae simplici et composito) pero que pudo haberse perdido por la
censura inquisitorial promulgada por el Papa Gregorio XI (Blanco et al.). Posterior a: “al
Liber de arte distillandit”, Berthelot encontró en un manuscrito del siglo XII indicios del
origen del alcohol en la obra intitulada “la Clave de la Pintura” (Miguéz, 1998) en la cuál
se explica la forma de fabricar el alcohol. Según el texto, se debe “mezclar vino fuerte y
puro con un tercio de su peso de sal y calentarlo en un recipiente apropiado, se obtiene
aún un agua inflamable que arde sin consumir el material donde se echa” (Blas, 1947).
Aunque son muy imprecisos, existen datos que sitúan a importantes personajes
explicando la forma como se fue destilando el alcohol: Abulcasis (el Zahravi) natural de
Córdoba, fue el autor del Metodus medeud, en el que se describe la forma como se debe
destilar el alcohol a partir del vinagre, lo anterior fue cerca al año 1000 de nuestra época
(Blas, 1947).
El dominio de los destilados duró hasta el siglo XVIII, cuando se comenzaron a
popularizar las infusiones con agua destilada de café, té y cacao.
Por el año de 1836, Juan Bautista Andrés Dumas agrupó bajo el nombre de alcoholes a
un grupo de sustancias obtenidas a partir del espíritu de la madera y el vino, estas
sustancias poseen propiedades similares al alcohol ordinario. Años más tarde, en 1860
Berthelot estableció las ocho funciones orgánicas entre las que se encontraba el alcohol
en segunda posición y como grupo distintivo se categorizó el oxhidrilo (Blas, 1947).
En el siglo XIX se da el descubrimiento de los microrganismos por parte de
“Louis Pasteur, que fue el fundador de la moderna tecnología del vino al
explicar la fermentación. Durante miles de años este proceso había sido un misterio insoluble. En 1857, Pasteur demostró que la fermentación era un
fenómeno biológico y que la levadura su agente, segrega un fermento
endógeno, una enzima que desdobla la glucosa en alcohol y carbónico”
(Miguéz, 1998).
A raíz del descubrimiento realizado por Pasteur, se comenzó a brindar un tratamiento
óptimo al agua, combatiendo directamente el papel patógeno de los microrganismos con
lo que se volvió potable. Por esta misma época se pudo definir la estructura molecular del
etanol.
El alcohol etílico se puede encontrar en bebidas alcohólicas, cosméticos, en tinturas y en
preparados farmacéuticos. El alcohol metílico (CH3OH), también conocido como alcohol
de madera, se emplea abiertamente como combustible y disolvente. El alcohol
isopropílico (CH3CH2OHCH3) se utiliza como antiséptico y desinfectante (Wade; 2004).
Debido a su versatilidad, el grupo hidroxilo, se puede sintetizar de múltiples formas, así
como también, se puede convertir en la mayoría de los grupos funcionales por múltiples
reacciones (Wade;2004).
Alcohol como agente desinfectante en tiempos de CORONA VIRUS
Con el término alcohol, nos referiremos a dos compuestos principales usados como agentes desinfectantes: el etanol (C2H5OH) o alcohol etílico, y el isopropanol o alcohol isopropílico ((CH3)2CHOH).
Su principal forma de acción antimicrobiana, es mediante la desnaturalización de las proteínas, permitiendo la ruptura de membranas. La acción microbicida del alcohol a diversas concentraciones ha sido examinada a una amplia variedad de especies, con periodos de exposición de 10 segundos a una hora. A concentraciones de 60%-80%, tanto el etanol como el isopropanol, son potentes agentes virucidas, inactivando casi todas las especies de virus lipofílicos y muchos de los virus hidrofílicos. Tiene una potente actividad antifúngica, incluyendo levaduras.
Los alcoholes no son recomendados para la esterilización de material médico o quirúrgico, debido principalmente a que es incapaz de dañar a microorganismos esporulados y no puede penetrar materiales ricos en proteínas. No se conocen resistencias desarrolladas por la exposición al etanol.
El alcohol es incoloro, pero volátil e inflamable, por lo tanto debe almacenarse en ambientes fríos y bien ventilados. Además se evaporan rápidamente, razón por la cual que es difícil tener periodos extendidos de exposición, a menos de que los materiales se encuentren sumergidos en el alcohol.
Para complementar esta información entra al siguiente link, observa los videos y lee el artículo completo:
LA IMPORTANCIA DEL JABÓN
Todos los días nuestras actividades comunes nos ponen en contacto con este químico, y sólo necesitamos saber que sirve para limpiar, que suele tener un olor agradable y que sus formas pueden ser variadas. Sin embargo, poca información poseemos respecto a su composición química. Este artículo refiere cómo, a través de la historia, el papel del jabón ha sido importante para el desarrollo de nuevas tecnologías, derivadas de las necesidades globales de la sociedad. El impacto de la demanda de este producto se observa en los métodos empleados para elaborarlo. La química detrás de este producto responde a varias incógnitas: ¿Cómo funciona un jabón? ¿Por qué hace burbujas? ¿Por qué limpia? ¿De dónde viene? ¿Por qué sus diferentes presentaciones? ¿Es lo mismo jabón y detergente?
Todo comienza con las grasas de origen animal o aceites vegetales (lípidos) que se transforman en jabones. No es cuestión de magia: Esto se llama química, e implica una reacción muy sencilla denominada saponificación. Un jabón contiene las sales de sodio o potasio de los ácidos grasos, producto de la mezcla de un cuerpo graso (triglicéridos con un álcali, que puede ser hidróxido de sodio o de potasio).
Las sales de potasio o de sodio son un grupo de compuestos del carbono que se obtienen por la reacción química entre un ácido carboxílico y una base o hidróxido.
Su grupo funcional es COO- y la nomenclatura IUPAC implica cambiar la terminación "ico" del ácido por "ato" y especificar de que metal es (potasio o sodio).
¿Cómo funciona un jabón?
Como si se tratara de una batería con polos positivo y negativo, una molécula de jabón también tiene dos extremos de diferente afinidad.
La Figura a continuación representa una molécula de jabón. En rojo, la cabeza, con carga, es afín al agua (hidrofílica) porque son de polaridad similar (-COOK; -COONa). La cadena azul, denominada lipofílica (cadena de carbonos e hidrógenos), es afín a las grasas y repele al agua. A causa de esta estructura, el jabón posee una doble afinidad hacia la polaridad de otras moléculas y puede orientarse según el medio donde se encuentre.
La Figura a continuación representa una molécula de jabón. En rojo, la cabeza, con carga, es afín al agua (hidrofílica) porque son de polaridad similar (-COOK; -COONa). La cadena azul, denominada lipofílica (cadena de carbonos e hidrógenos), es afín a las grasas y repele al agua. A causa de esta estructura, el jabón posee una doble afinidad hacia la polaridad de otras moléculas y puede orientarse según el medio donde se encuentre.
¿Cómo explicar desde la química del jabón lo que sucede en este video que circula en twitter ?
TENSIÓN SUPERFICIAL
TAREA
REPITE Y COMPRUEBA LA EXPERIENCIA EN TU HOGAR Y GRABA TU PROPIO VIDEO EXPLICATIVO
Los jabones limpian debido a las afinidades diferentes de los extremos de sus moléculas. La suciedad grasa no se elimina fácilmente sólo con agua, que la repele por ser insoluble en ella. Sin embargo, el jabón posee una cadena larga alifática o hidrocarbonada sin carga que interactúa con la grasa, disolviéndola, mientras que la región con carga se orienta hacia el exterior, formando gotas. Una vez que la superficie de la gota grasa está cubierta por muchas moléculas de jabón, se forma una micela con una pequeña gota de grasa en el interior. Esta gota de grasa se dispersa fácilmente en el agua, ya que está cubierta por las cabezas con carga o aniones carboxilato del jabón, como se observa en la figura de abajo. La mezcla que resulta de dos fases insolubles (agua y grasa), con una fase dispersada en la otra en forma de pequeñas gotas, se denomina emulsión. Por lo tanto, se dice que la grasa ha sido emulsionada por la solución jabonosa. De esta manera, en el proceso de lavado con un jabón, la grasa se elimina con el agua del lavado.
...y entonces
¿cómo actúa entonces el jabón con los virus ?
RECUERDA:
"ESTA BATALLA LA GANAMOS CON AGUA Y JABÓN"